2026-02-10 19:55:33
1月31日至2月6日,醫藥生物指數下跌2.71%,跑輸上證指數,創新藥賽道展現韌性。丹諾醫藥二次遞表港交所,其核心產品利福特尼唑預計2026年獲批上市。云頂新耀口服自免藥物維適平獲批,用于治療潰瘍性結腸炎。強生登記一項II期肺癌臨床試驗,探索新治療方案,若成功將拓展免疫治療獲益人群。
每經記者|金喆 每經編輯|魏官紅
一周行情
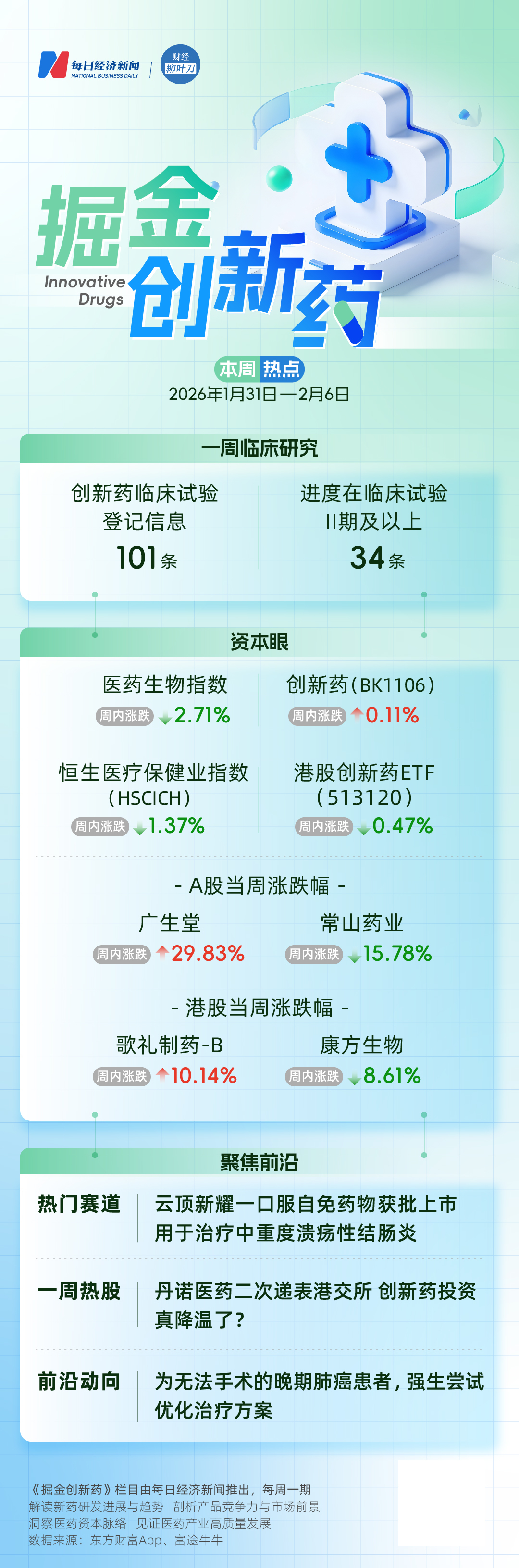
1月31日至2月6日,醫藥生物指數下跌2.71%,跑輸上證指數1.44個百分點。創新藥(BK1106)周內上漲0.11%,恒生醫療保健業指數(HSCICH)周內下跌1.37%;港股創新藥ETF(513120)周內下跌0.47%。
一周點評
上周醫藥生物板塊整體走弱跑輸滬指,創新藥賽道展現相對韌性,港股醫療相關指數跌幅收窄,板塊內部分化由個股基本面與事件催化主導。廣生堂因乙肝藥III期臨床入組完成,疊加中西醫結合治乙肝的國家級政策利好,股價大幅領漲;常山藥業受商業賄賂觸發集采信用風險、2025年業績預虧等利空影響,成為A股領跌標的。港股方面,歌禮制藥-B獲GIC大額增持,募資將用于GLP-1管線研發,帶動股價上行;康方生物因核心雙抗產品FDA審批標準趨嚴、短期缺乏業績與管線催化,股價顯著下挫。
2026年初至今,醫藥行業整體上漲3.28%、跑贏滬深300指數,細分賽道結構性景氣凸顯,醫院、線下藥店、醫藥研發外包位列漲幅前三,分別錄得12.3%、10.6%、8.8%的漲幅,消費醫療需求復蘇與創新藥研發高增成為核心驅動。
一周新股動向
丹諾醫藥二次遞表港交所 創新藥投資真降溫了?
2月3日,丹諾醫藥(蘇州)股份有限公司(以下簡稱“丹諾醫藥”)向港交所主板遞交了上市申請。《每日經濟新聞》記者注意到,2025年7月30日,丹諾醫藥曾向港交所首次遞交上市申請,但申請屆滿6個月后,已于2026年1月28日失效。隨后,丹諾醫藥發起第二次上市沖刺。
招股書顯示,丹諾醫藥目前有7個在研產品,公司將利福特尼唑(TNP-2198)和利福喹酮(TNP-2092注射劑)定義為核心產品。其中,利福特尼唑(口服)是一款廣譜雙靶點小分子藥物,也是自1982年發現幽門螺桿菌以來,全球首個且唯一治療該細菌感染的新分子實體候選藥物。資料顯示,利福特尼唑(口服)最快預計2026年在中國獲批上市,這也是丹諾醫藥進度最快的一款產品。
業績方面,2023年、2024年及2025年前9個月,公司分別錄得凈虧損1.92億元、1.46億元及1.15億元,主要由于產生大量的研發開支。
據了解,馬振坤是丹諾醫藥的董事會主席、執行董事、首席執行官兼總經理,在傳染病領域的新藥開發方面擁有逾30年經驗。
丹諾醫藥的二次遞表,恰是當前創新藥投資環境的縮影,并未“退潮”,只是資本更理性——不再為“賽道熱度”買單,而是聚焦“臨床落地能力”與“生存韌性”。我們也可以看到,過去港股18A板塊依賴“管線數量”“概念新穎度”估值的邏輯已失效,如今投資者更看重三大核心:臨床確定性(如利福特尼唑的獲批進度)、商業化可行性(是否有明確合作方與醫保路徑)以及現金流健康度(現金能否支撐至產品上市)。
一周臨床試驗動向
根據醫藥魔方提供的數據,1月31日至2月6日,國家藥品監督管理局藥品審評中心共披露101條臨床試驗登記信息,其中34條為處于臨床試驗II期及以上的創新藥新登記臨床試驗信息,3個臨床研究項目正在招募患者。
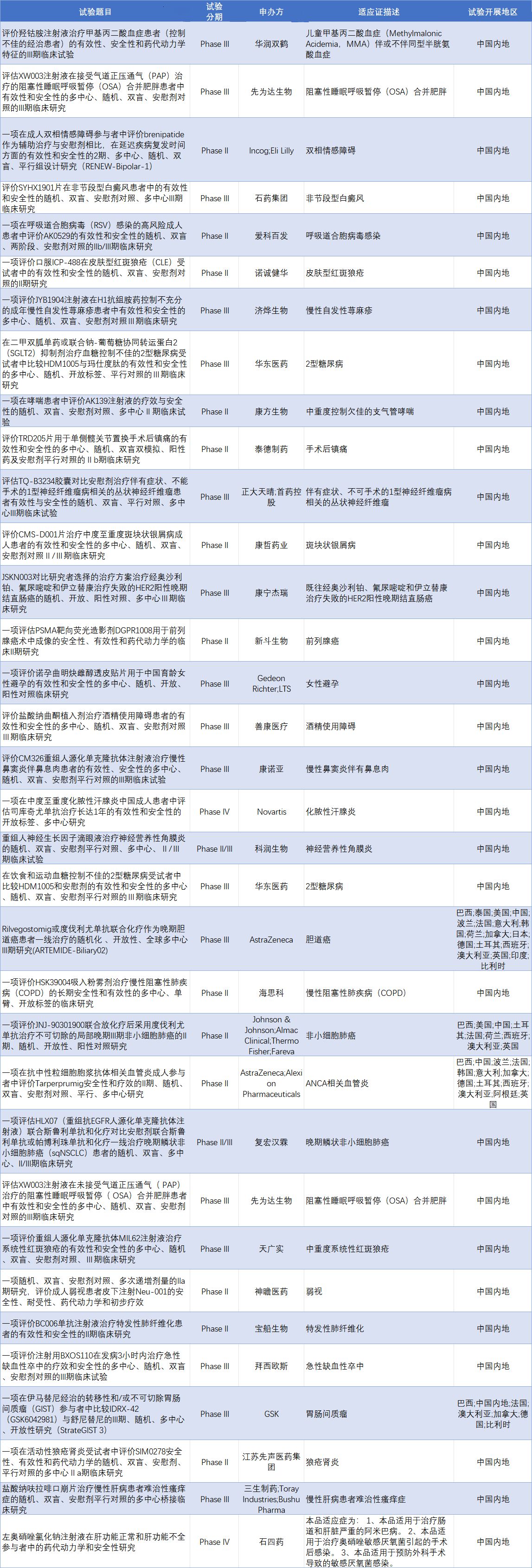
數據來源:醫藥魔方
本周,有3款創新藥獲批。
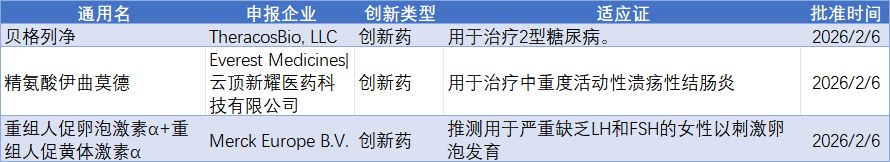
數據來源:醫藥魔方
云頂新耀一口服自免藥物獲批上市 用于治療中重度潰瘍性結腸炎
2月6日,云頂新耀(1952.HK)宣布,其自身免疫性疾病領域產品維適平(精氨酸艾曲莫德片)獲得中國國家藥品監督管理局批準上市,用于治療對傳統治療或生物制劑應答不充分、失應答或不耐受的中度至重度活動性潰瘍性結腸炎(UC)成人患者。
近年來,中國潰瘍性結腸炎發病率持續上升,并呈現年輕化趨勢,預計患者人數將由2025年的約98萬增長至2031年的約150萬。然而,長期以來,我國潰瘍性結腸炎治療面臨傳統療法療效有限、復發率高、給藥便捷性差以及不良反應多等諸多局限。
每經記者了解到,對于潰瘍性結腸炎患者來說,其核心治療需求是持續的癥狀緩解,“病情長期穩定、無激素依賴”是改善患者生活質量的關鍵目標。但黏膜愈合作為國內外權威指南及共識一致明確的UC核心治療目標,長期面臨達標率偏低、臨床推進難度大的困境。《中國IBD藍皮書:中國炎癥性腸病醫患認知暨生存質量報告》顯示,臨床實踐中,僅24%的UC患者達到內鏡下黏膜愈合,遠未滿足臨床需求。
另有研究數據顯示,約五分之一的患者因病情無法正常工作或學習,長期反復發作還可能誘發焦慮、抑郁等心理問題,而患病10年以上的患者,更面臨結直腸癌變的額外風險,使其成為威脅患者身心健康的系統性疾病。
云頂新耀方面表示,維適平是新一代高選擇性S1P受體調節劑,每日一次口服,可實現快速起效和強效深度黏膜愈合,并具有良好的安全性特征。記者還注意到,今年1月,艾伯維宣布白介素-23(IL-23)特異性抑制劑利生奇珠單抗也獲批了可用于上述適應證。
針對無法手術的晚期非小細胞肺癌患者,強生嘗試優化治療方案
醫藥魔方數據顯示,2月2日,強生登記一項II期肺癌臨床試驗,核心為評估JNJ-90301900(即NBTXR3)聯合放化療后,序貫度伐利尤單抗鞏固治療不可切除局部晚期III期非小細胞肺癌(NSCLC)的療效與安全性。該研究是對不可切除III期NSCLC標準治療方案的升級探索,目標入組130人。
每經記者注意到,目前全球不可切除局部晚期III期NSCLC的標準根治性治療模式,是由阿斯利康的PD-L1抑制劑度伐利尤單抗的III期PACIFIC臨床試驗結果確立——先完成以鉑類為基礎的同步放化療(根治性放化療),經評估確認疾病無進展后,序貫使用度伐利尤單抗進行免疫鞏固治療,標準鞏固治療時長為12個月。
該模式自2018年起,被NCCN(美國國立綜合癌癥網絡)、CSCO(中國臨床腫瘤學會)等全球各大肺癌診療指南列為I類推薦。后續所有探索該適應證升級方案的臨床試驗,都以PACIFIC模式為陽性對照標桿。若強生發起的此次研究取得陽性結果,將有望為不可切除III期NSCLC患者提供“放療增敏+免疫鞏固”的全新治療策略,進一步拓展免疫治療的獲益人群。
10倍價差刷屏!“外國人來華就醫”火了,三位親歷者這樣說??
進入2026年以來,“外國人來華就醫”突然成為全球互聯網上的高頻熱詞。
英國網紅博主艾米(Amie)在其國家候診兩年,而在中國僅用13天便完成了診療全程。她還拍攝視頻分享了在中國的就醫情況,感慨中外診療費用差距高達10倍。
在一些社交平臺,不少外國博主也紛紛曬出在中國醫院就診的感受:“我將向所有人推薦中國的醫療,真是太棒了”“中國的醫院效率高得可怕”“中國的醫院再一次讓人震驚”??
這一幕讓很多中國人有些恍惚:有錢人不是都傾向于去歐美發達國家看病嗎?自己習以為常的中國醫療,為何在全球竟成了又快、又好、又實惠的典范?
據南方日報,2025年國內重點涉外醫院全年接診的國際患者達128萬人次,該數字較三年前猛增73.6%。另據中國醫院協會國際醫療服務專委會報告,2024年全國已有57個城市的850家醫療機構開設了國際醫療服務,形成了一個初具規模的生態網絡。
沒有什么比親身經歷更具說服力。近日,《每日經濟新聞》記者與外國患者、中國醫生以及海外醫療服務機構取得聯系,他們分享了自己就醫或協助他人就醫的故事。這些故事充分表明,中國醫療在全球坐標系下的競爭力日益提升,正影響著越來越多的人。

如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
